Преферанская Нина Германовна
Доцент кафедры фармакологии фармфакультета ММА им. И.М. Сеченова, к.фарм.н.
При повреждении мелких сосудов кровотечение у человека останавливается через 1-3 минуты. Скорость и процесс свертывания крови зависит от синтеза, биоактивности и концентрации ее факторов [фибриноген (фактор I), протромбин (фактор II), тромбопластин (фактор III), кальций (фактор IV), проконвертин (фактор VII), фактор IX и фактор Х].
ГЕМОСТАТИЧЕСКИЕ СРЕДСТВА
Гемостатики применяются при заболеваниях, сопровождающихся пониженной свертываемостью крови (гемофилия, тромбоцитопеническая пурпура и др.), для остановки кровотечений (желудочных, кишечных, геморрагических, легочных, маточных), а также профилактически перед хирургическими операциями для снижения кровопотери в момент самой операции. Их используют в быту при незначительных мелких повреждениях кожи. Средства данной группы нередко представляют собой естественные компоненты системы свертывания крови — тромбин, фибриноген, соли кальция, витамин К.
В зависимости от применения они делятся на препараты для системного
применения и местного действия
Гемостатики (коагулянты) также классифицируют на препараты:
- необходимые для образования факторов свертывания крови — препараты витамина К и его производные (Менадион, Викасол, Фитоменадион);
- резорбтивного действия — фибриноген, соли кальция;
- компоненты факторов свертывания крови — антигемофильный Фактор VIII, Криопреципитат, Фактор IX комплекс;
- с гемостатическими свойствами — Дицинон (Этамзилат), Эритрофосфатид;
- антагонисты гепарина — Протамина сульфат;
- блокирующие процесс фибринолиза — Ингибиторы фибринолиза (антифибринолитические);
- местного действия: Тромбин, Губка гемостатическая, Желпластин, Желатиноль;
- растительного происхождения — Водяного перца трава, Лагохилус опьяняющий, Крапивы лист, Пастушьей сумки трава, Горца почечуйного трава.
ПРЕПАРАТЫ ВИТАМИНА K
Витамин К существует в виде двух форм — витамина K1 (филлохинон), обнаруженного в растениях, и витамина К2 — группа соединений (менахиноны), синтезируемых микроорганизмами (в частности, микрофлорой кишечника человека). Витамины K1 и K2 — это жирорастворимые соединения, которые являются производными 2-метил-1,4-нафтохинона и различаются по длине и характеру боковой углеродной цепи. Витамин K1 получен синтетическим способом, его препарат известен под названием Фитоменадион. Синтезирован водорастворимый предшественник витамина К — 2-метил-1,4-нафтохинон (менадион), обладающий провитаминной активностью. Это соединение было названо витамином К3. Производное витамина К3 — менадиона натрия бисульфит используется в медицинской практике под названием Викасол.
Витамин К необходим для синтеза протромбина (фактора II) и факторов свертывания крови VII, IX и Х в печени. Известно участие витамина К в синтезе белка костной ткани остеокальцина. Структура всех витамин К-зависимых-карбоксиглутаминовых белков имеет общую особенность — эти белки содержат остатки g-карбоксиглутаминовых кислот, которые связывают ионы Са2+. Витамин К — гидрохинон является коферментом в реакции остатков глутаминовых кислот. При недостаточности в организме витамина К в крови появляются неактивные предшественники факторов свертывания крови, вследствие чего дефицит витамина К в организме очень быстро приводит к нарушению свертывания крови. Поэтому основными и наиболее ранними проявлениями К-витаминной недостаточности являются кровотечения и кровоизлияния.
Препараты витамина К используют для предупреждения и остановки кровотечений, при геморрагических осложнениях, вызванных недостаточностью витамина К в организме. Так, эти препараты применяют при геморрагическом синдроме новорожденных. К-авитаминоз у новорожденных может быть вызван как недостаточным поступлением витамина K1, так и отсутствием микрофлоры кишечника, синтезирующей витамин К2. Для предупреждения таких осложнений рекомендуется профилактическое введение витамина K новорожденным в первые часы жизни. Препараты показаны при снижении всасывания витамина К в кишечнике, что может быть связано с нарушением выделения желчи при обтурационной желтухе (желчь необходима для всасывания жирорастворимого витамина К) или с синдромом мальабсорбции (при спру, энтероколитах, болезни Крона и др.). Эффективны препараты витамина Kи при кровотечениях, вызванных антикоагулянтами непрямого действия, их вводят внутрь и внутривенно медленно.
Препараты витамина К могут вызывать аллергические реакции (сыпь, зуд, эритема, бронхоспазм). При внутривенном введении возникает риск анафилактоидных реакций. При применении Викасола у новорожденных существует опасность развития гемолитической анемии и гипербилирубинемии.
ПРЕПАРАТЫ РЕЗОРБТИВНОГО ДЕЙСТВИЯ
Фибриноген является составной частью крови, поэтому его получают из плазмы крови человека. В организме под влиянием тромбина он превращается в фибрин. Фибриноген применяют при кровотечениях, обусловленных пониженным содержанием его в крови. Это возникает при заболеваниях печени, когда нарушается синтез фибриногена или при усиленном лизисе, во время массивных кровопотерь, когда активируется система фибринолиза. Показаниями к назначению фибриногена являются кровотечения, возникающие во время операций на органах, богатых тканевыми активаторами фибринолитической системы (легкие, поджелудочная, предстательная, щитовидная железы). Используется при травматическом, ожоговом, трансфузионном шоке, для остановки кровотечений у больных гемофилией, а также в акушерской практике при преждевременной отслойке плаценты, внутриутробной гибели плода, кесаревом сечении. При многократном введении фибриногена могут наблюдаться явления сенсибилизации.
ПРЕПАРАТЫ КАЛЬЦИЯ
Кальций — обязательный участник процесса свертывания крови. Он активирует фермент тромбопластин и способствует образованию тромбина. Под влиянием кальция повышается агрегация тромбоцитов. Кроме того, ионы кальция уплотняют стенку капилляров и участвуют в процессе сужения сосудов. Соли кальция — Кальция хлорид, Кальция глюконат и Кальция лактат — применяются при легочных, желудочно-кишечных, носовых, маточных кровотечениях, а также при повышенной проницаемости сосудов (геморрагический васкулит) и для устранения, профилактики осложнений при оперативных вмешательствах. Кальция хлорид назначают внутрь и внутривенно капельно или вводят методом электрофореза. Растворы нельзя вводить подкожно и в/м, т.к. они вызывают сильное раздражение и некроз тканей. Сравнительно с кальцием хлоридом, соли Глюконата и Лактата лучше переносятся, т.к. местно в меньшей степени раздражают слизистую оболочку и могут применяться внутрь в таблетках.
Этамзилат (Дицинон) увеличивает скорость образования первичного тромба в пораженном сосуде, активируя образование тканевого тромбопластина. Кратковременно увеличивает свертываемость крови, выраженный эффект проявляется в зависимости от начальной скорости свертывания. Препарат наиболее эффективен при паренхиматозных, капиллярных и вторичных кровотечениях. Его используют для лечения геморрагического синдрома. При в/в введении противогеморрагический эффект наступает через 5-15 мин. и продолжается 6 час. После курсового лечения (при приеме внутрь) эффект сохраняется неделю. По активности уступает транексамовой кислоте. Препарат по фармакологической классификации относят к ангиопротекторам, т.к. в эндотелии сосудов снижает образование простациклина, повышает резистентность и нормализует проницаемость капилляров. Хорошо переносится, не вызывает выраженной гиперкоагуляции, при длительном применении не способствует развитию флебитов, тромбозов и эмболий. Может вызвать снижение артериального давления и головную боль.
ПРЕПАРАТЫ ФАКТОРОВ СВЕРТЫВАНИЯ КРОВИ
Необходимость в таких препаратах возникает при недостаточности одного или нескольких факторов свертывания крови. Все препараты факторов свертывания, получаемые из плазмы крови, имеют существенный недостаток — возможность передачи вирусных инфекций (ВИЧ, гепатита). В настоящее время получены рекомбинантные препараты фактора VIII и фактора Виллебранда, применение которых снижает риск инфицирования.
Антигемофильный фактор VIII (Гемофил М, Иммунат, Коэйт XII) представляет собой очищенную лиофилизированную фракцию человеческой плазмы, содержащую фактор VIII. Препараты фактора VIII вводят внутривенно при наследственной (гемофилия А) и приобретенной недостаточности фактора VIII.
Криопреципитат — концентрат белков плазмы крови, в состав входят: фактор VIII, фактор Виллебранда, фибриноген. Криопреципитат используют для заместительной терапии при болезни Виллебранда (наследственная недостаточность фактора Виллебранда) и афибриногенемии.
Концентрат факторов протромбинового комплекса — Фактор IX комплекс (Иммунин, Конайн 80, Октанайн, Аимафикс), представляющий собой очищенную фракцию человеческой плазмы, обогащенную фактором IX, применяют при врожденном (гемофилия В) и приобретенном дефиците фактора IX, а также при передозировке антикоагулянтов непрямого действия.
При введении этих препаратов могут появиться побочные реакции в виде тахикардии, артериальной гипотензии, одышки. Возможны аллергические реакции — крапивница, повышение температуры тела, анафилактический шок, а также гемолиз эритроцитов.
Кроме препаратов факторов свертывания, при легкой форме гемофилии А и болезни Виллебранда применяют аналог аргинин-вазопрессина Десмопрессин (Адиуретин). Десмопрессин повышает уровень фактора Виллебранда в плазме крови, способствуя его выделению из эндоплазматического ретикулума эндотелиальньк клеток, и увеличивает активность фактора VIII в плазме крови. Препарат вводят парентерально.
В качестве гемостатических средств используются компоненты крови: свежезамороженная плазма, плазма нативная концентрированная или плазма бесцитратная.
Антидот гепарина — протамина сульфат. Препарат белкового происхождения, содержит аргинин, аланин, пролин, серин и другие аминокислоты. Препарат нейтрализует противосвертывающее действие гепарина, образуя нерастворимые стабильные комплексы. Активность выражается в ЕД, в 1 мл 1% раствора содержится не менее 750 ЕД. 75 ЕД протамина сульфата нейтрализует 85 ЕД гепарина. Препарат вводят в/в струйно или капельно, под контролем показателей свертывания крови. Эффект развивается через 1-2 мин. и продолжается около 2 часов. При приеме внутрь он разрушается. При применении этого препарата необходимо правильно рассчитать дозу, т.к. возможны выраженные нарушения свертываемости и усиление кровотечения.
СРЕДСТВА, ДЕЙСТВУЮЩИЕ НА ПРОЦЕССЫ ФИБРИНОЛИЗА
При образовании тромбов происходит активация фибринолитической системы, которая обеспечивает растворение (лизис) фибрина и разрушение тромба. Это приводит к восстановлению нормального кровотока. В процессе фибринолиза происходит превращение неактивного плазминогена в плазмин (фибринолизин) при участии активаторов плазминогена. Плазмин гидролизует фибрин с образованием растворимых пептидов. Плазмин не обладает специфичностью и вызывает также разрушение фибриногена и некоторых других факторов свертывания крови. Это повышает риск развития кровотечений. Плазмин (циркулирующий в крови) быстро инактивируется α2-антиплазмином и другими ингибиторами, поэтому в норме не оказывает системного фибринолитического действия. Однако при определенных патологических состояниях или применении фибринолитических средств возможна чрезмерная активация системного фибринолиза, что может стать причиной кровотечений.
Для остановки кровотечений, вызванных повышенной активностью фибринолитической системы, при травмах, хирургических вмешательствах, родах, заболеваниях печени, простатитах, меноррагиях, а также при передозировке фибринолитических средств, применяются антифибринолитические средства.
Для этих целей используют препараты, которые ингибируют активацию плазминогена или являются ингибиторами плазмина. Антифибринолитические средства различают в зависимости от происхождения на препараты синтетические: аминокапроновая кислота (амикар), аминометилбензойная кислота (амбен, памба); тканевого происхождения — апротинин (гордокс, контрикал, трасилол) и пантрипин.
Аминокапроновая кислота связывается с плазминогеном и препятствует его превращению в плазмин. Кроме того, препарат препятствует действию плазмина на фибрин, нормализует уровень фибриногена и не вызывает резкой гиперкоагуляции. При его применении восстанавливается время свертывания крови и тромбиновое время до нормальных показателей. Вводят внутрь (4-5 г одномоментно, далее 1 г каждые 4 часа) и внутривенно (не более 250 мг/мл) с изотоническим раствором натрия хлорида или раствором глюкозы или белковых гидрализатов. Возможны побочные эффекты — тошнота, диарея, артериальная гипотензия, брадикардия, аритмии, головокружение, судороги, нарушение слуха, аллергические реакции.
Аминометилбензойная кислота (амбен, памба) по строению и механизму действия близка к аминокапроновой кислоте, но более активна. Угнетает фибринолиз путем конкурентного торможения плазминогенактивируюшего фермента и подавления образования плазмина. Применяется внутрь, в/в, в/м, иногда введение сочетают с противошоковыми жидкостями или препаратами для парентерального питания.
Транексамовая кислота (транексам, циклокапрон) является конкурентным ингибитором активатора плазминогена. Препарат вводят внутрь и внутривенно. По эффективности превосходит аминокапроновую кислоту, действуя более продолжительно. Антифибринолитическая концентрация в крови сохраняется 7-8 часов, в различных тканях организма до 17 часов. При применении транексамовой кислоты происходит торможение образования кининов и других пептидов, поэтому она обладает противовоспалительными и противоаллергическими свойствами. Однако может вызывает диспептические явления (анорексия, тошнота, рвота, диарея), головокружение, сонливость. Иногда возможны кожные аллергические реакции.
Апротинин (Гордокс, Контрикал, Трасилол, Ингитрил) ингибирует плазмин и другие протеолитические ферменты. Препарат вводят внутривенно. Побочные эффекты: артериальная гипотензия, тахикардия, тошнота, рвота, аллергические реакции.
Кроме того, для остановки маточных, легочных, почечных, кишечных и других кровотечений используют препараты лекарственных растений — листья крапивы, траву тысячелистника, траву горца почечуйного, кору калины, цветки арники, лагохилус опьяняющий, лист подорожника. Применяют лекарственные растения в виде настоев, настоек и экстрактов внутрь и местно.
Преферанская Н.Г.
Гемостатические средства
Гемостатические средства — лекарственные средства, способствующие остановке кровотечений. Все гемостатики, в зависимости от механизма действия, подразделяются на три большие группы:
- ингибиторы фибринолиза (антифибринолитики);
- средства, усиливающие свертывание крови (коагулянты);
- средства, понижающие сосудистую проницаемость.
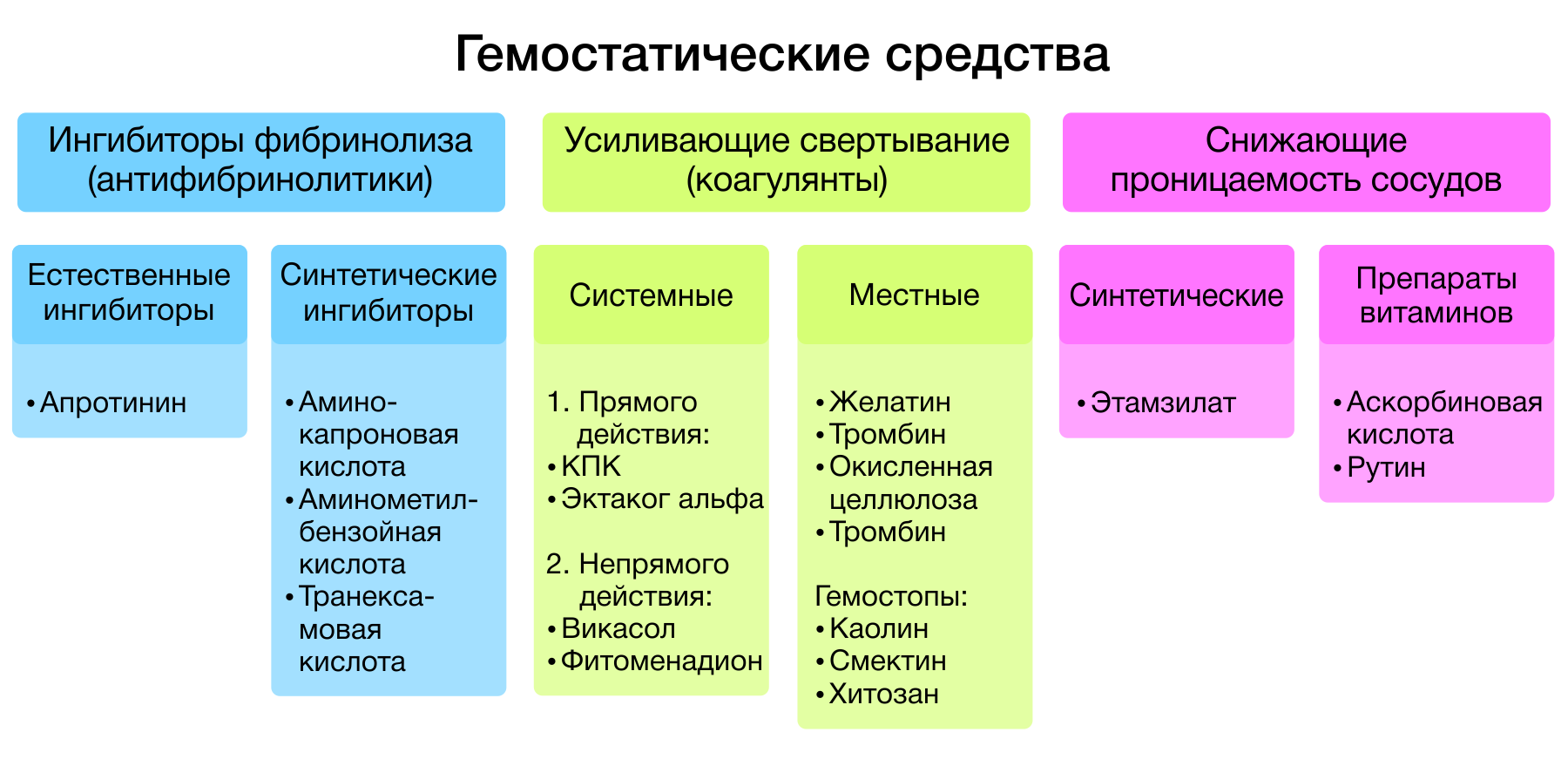
Рисунок 1 | Классификация гемостатиков.
1. Ингибиторы фибринолиза.
В клинической практике широкое распространение получили две группы препаратов ингибиторов фибринолиза: естественные ингибиторы фибринолиза (апротинин и его аналоги) и синтетические ингибиторы фибринолиза (аминокапроновая кислота, аминометилбензойная кислота, транексамовая кислота).
Апротинин — полипептид, получаемый из легких, поджелудочной и околоушной желез крупного рогатого скота, действующий аналогично α2-антиплазмину. Апротинин разрушает свободный плазмин, практически не взаимодействует со связанным плазмином, а также угнетает активацию тромбоцитов. Являясь сериновой протеазой, апротинин блокирует калликреин-кининовую систему путем разрушения калликреина, снижает активность отдельных протеолитических ферментов, таких как: трипсин, химотрипсин, кининогеназа. Изначально препарат был включен в рекомендации по лечению острого панкреатита и панкреонекроза, однако не подтвердил свою эффективность, и показания к его применению были пересмотрены.[1]
Аминокапроновая кислота — 6-аминогексановая кислота — синтетическое производное лизина. Присоединяясь к лизин-связывающему участку плазминогена, аминокапроновая кислота обратимо блокирует процесс фибринолиза, снижает активность стрептокиназы, урокиназы, тканевых киназ, калликреина, трипсина и гиалуронидазы. Аналогичным фармакологическим эффектом обладает производное аминокапроновой кислоты — аминометилбензойная кислота, отличающаяся улучшенной фармакокинетикой. Аминокапроновая кислота снижает активность тромболитических препаратов и может быть использована для нейтрализации их эффекта.
Транексамовая кислота — транс-4-(аминометил)-циклогексанкарбоновая кислота — обратимо блокирует эффект плазминогена, адгезию лейкоцитов и тромбоцитов на поверхность тромба за счет конкурентного ингибирования активатора плазминогена. Оказывает противоаллергическое и противовоспалительное действие посредством подавления образования кининов и других активных пептидов, участвующих в аллергических и воспалительных реакциях. По мощности антифибринолитического действия транексамовая кислота значительно превосходит аминокапроновую кислоту. Активность препарата в плазме сохраняется на протяжении 7-8 часов, в тканях — до 17 часов.[2]
У больных с высоким риском массивной кровопотери в плановой хирургии (сердечно-сосудистая хирургия, травматология и ортопедия, трансплантология) применение ингибиторов фибринолиза уменьшает интраоперационную кровопотерю и снижает потребность в трансфузии донорской крови. На протяжении 20 лет проводилось множество исследований, результаты которых были неоднозначны: мнения склонялись то в пользу апротинина, то в пользу синтетических производных лизина.
В 2007 году компания Bayer завершила исследование BART (Blood conservation using antifibrinolytics in a randomized trial), в котором было изучено действие апротинина у кардиохирургических больных высокого риска. Исследователи выявили большой риск летальных исходов и осложнений при использовании апротинина. В группе апротинина количество больных с массивной кровопотерей было несколько меньше, но 30-дневная летальность на 50% превышала аналогичный показатель в других группах.[3]
После публикации результатов BART компания Bayer уведомила Управление по контролю за качеством пищевых продуктов и лекарственных средств США (FDA) о намерении изъять апротинин с рынка. Показания к назначению были пересмотрены, и препарат был исключен из списка безопасных лекарственных средств.
Огромный мета-анализ позволил сделать вывод, что транексамовая кислота обеспечивает такое же снижение периоперационной трансфузии, какое наблюдается при использовании апротинина, но более безопасна. Согласно рекомендациям Европейского общества анестезиологов по ведению пациентов с массивной периоперационной кровопотерей (2013 г.), при массивном кровотечении рекомендуется применение транексамовой кислоты (20-25 мг/кг); она может быть введена повторно или применяться в виде пролонгированной инфузии (1-2 мг/кг/ч).[4]
2. Препараты, усиливающие свертывание крови
Среди средств, повышающих скорость свертывания крови, выделяют: средства системного действия и для местного применения. К препаратам системного действия относят непрямые коагулянты (фитоменадион, менадиона натрия бисульфит) и коагулянты прямого действия (факторы свертывания: концентрат протромбинового комплекса, эптаког альфа).
Менадиона натрия бисульфит — синтетический водорастворимый аналог витамина К3. Субстратно стимулирует витамин K-редуктазу, активирующую витамин К и обеспечивающую его участие в печеночном синтезе витамин K-зависимых плазменных факторов гемостаза (II, VII, IX, X). Фитоменадион является синтетическим структурным аналогом витамина К1, обладает большей активностью и более ранним началом реализации эффектов (через 6-10 часов после перорального применения, против 18-24 часов у менадиона натрия бисульфита). Данная группа препаратов показана для коррекции нарушений системы гемостаза, вызванных дефицитом витамина К1, передозировкой антикоагулянтов непрямого действия (варфарина), а также для предоперационной профилактики кровотечений.
Концентрат протромбинового комплекса (КПК) — лекарственный препарат, содержащий факторы II, VII, IX, X, а также следовые концентрации антитромбина III, гепарина, протеинов С и S. Основным показанием к применению КПК служит коррекция приобретенного дефицита витамин К1-зависимых факторов в экстренных ситуациях (кровотечение, экстренная операция). Помимо этого, КПК широко используется как средство для лечения и профилактики кровотечений у пациентов с врожденным дефицитом одного из К1 зависимых факторов свертывания (врожденная гипопротромбинемия, врожденный дефицит фактора Стюарта — Прауэра).[5]
Эптаког альфа — рекомбинантный активированный VII фактор свертывания. Механизм действия препарата заключается в прямой активации фактора Х на поверхности активированных тромбоцитов. Это вызывает «тромбиновый взрыв» независимо от имеющейся концентрации факторов VIIIa и IXa. В результате образуется стабильный фибриновый сгусток. Считается, что эптаког альфа инициирует гемостаз только в месте повреждения ткани и не вызывает системной активации механизмов свертывания. Препарат был разработан для лечения кровотечений и проведения хирургических вмешательств у пациентов с наследственной или приобретенной гемофилией и высоким титром ингибитора факторов свертывания VIIIa или IXa. Его применение у пациентов с массивным кровотечением можно сформулировать согласно рекомендациям ESA (2013): «Применение рекомбинантного фактора VII возможно только при кровотечениях, которые не могут быть устранены хирургическими методами или путем комплексной гемостаз-корригирующей терапии». Необходимо серьезное обоснование для применения данного препарата [6].
3. Местные гемостатики
Местные гемостатики используются для остановки капиллярных и паренхиматозных кровотечений преимущественно в неотложной хирургии и стоматологии. Данная группа включает в себя широкий спектр препаратов с различным механизмом действия.
Препараты на основе желатина, получаемого из свиной кожи, существуют в трех формах: пленка, губка и порошок. Желатин чрезвычайно гигроскопичен, и за счет этого свойства он абсорбирует влагу, увеличиваясь в размерах и заполняя тканевой дефект. Существуют комбинации желатина с тромбином, которые помимо пассивного гемостатического эффекта напрямую запускают коагуляционный каскад и активируют тромбоциты в месте нанесения. Желатин разрушается протеиназами в течение 4-6 недель. Несмотря на абсолютную индифферентность, желатин может служить в качестве хронического очага инфекции. Помимо этого, одним из существенных недостатков данных препаратов является отсутствие прочных связей с окружающими тканями [7].
Тромбин является естественным компонентом свертывающей системы крови. Раствор тромбина используют только местно при капиллярных или паренхиматозных кровотечениях в ходе нейрохирургических вмешательств, операций на печени и почках, в стоматологической практике. Попадание тромбина в крупные кровеносные сосуды может вызвать распространенный тромбоз [7].
Окисленная целлюлоза выпускается в виде пленок, сеток, пучков и губок. Данный биологический агент играет роль субстрата для агрегации тромбоцитов и активации механизмов гемостаза. Целлюлоза значительно снижает рН среды, что приводит к лизису эритроцитов с образованием кислого гематина, который формирует дополнительный искусственный сгусток. Помимо этого окисленная целлюлоза обладает антибактериальным эффектом, в том числе в отношении антибиотикорезистентных микроорганизмов [7].
Микрофибриллярный коллаген, производимый из кожи крупного рогатого скота, имеет ряд преимуществ перед остальными топическими биологическими кровоостанавливающими агентами, среди которых: быстрый гемостатический эффект, минимальная реактивность тканей и высокая способность к реабсорбции. Аналогично целлюлозе, микрофибриллярный коллаген является матрицей для активации тромбоцитов, агрегации и образования тромбов [7].
Подвидом местных кровоостанавливающих средств являются гемостопы, получившие большое распространение в военной медицине. Это препараты внешнего воздействия, которые почти не влияют на свертывающую и противосвертывающую системы крови. Многообразие форм выпуска обеспечивает удобство применения в полевых условиях и полностью удовлетворяет потребностям оказания неотложной помощи при любых кровотечениях. На сегодняшний день наиболее эффективным средством считается хитозан.
Хитозан — это полисахаридный биополимер, получаемый из хитиновых панцирей ракообразных. Кровоостанавливающий эффект данного вещества достигается путем связывания хлопьев хитозана с отрицательно-заряженными эритроцитами и образования гелеобразного сгустка в месте контакта с кровью. Среди преимуществ препаратов на основе хитозана выделяют его антимикробные свойства, длительный срок хранения, стабильность при перепадах температур и безопасность при наружном использовании [8].
Наиболее известным представителем группы средств, понижающих сосудистую проницаемость, является этамзилат. Гемостатический эффект данного препарата обусловлен активацией тромбопластина в месте повреждения сосудов микроциркуляторного русла и снижением синтеза простациклина PGI-2 в эндотелии сосудов, что в конечном итоге приводит к усилению адгезии и агрегации тромбоцитов, остановке или уменьшению кровоточивости. За счет антигиалуронидазного действия этамзилат обладает ангиопротективным эффектом, улучшает микроциркуляцию и нормализует проницаемость сосудистой стенки при патологических процессах [9].
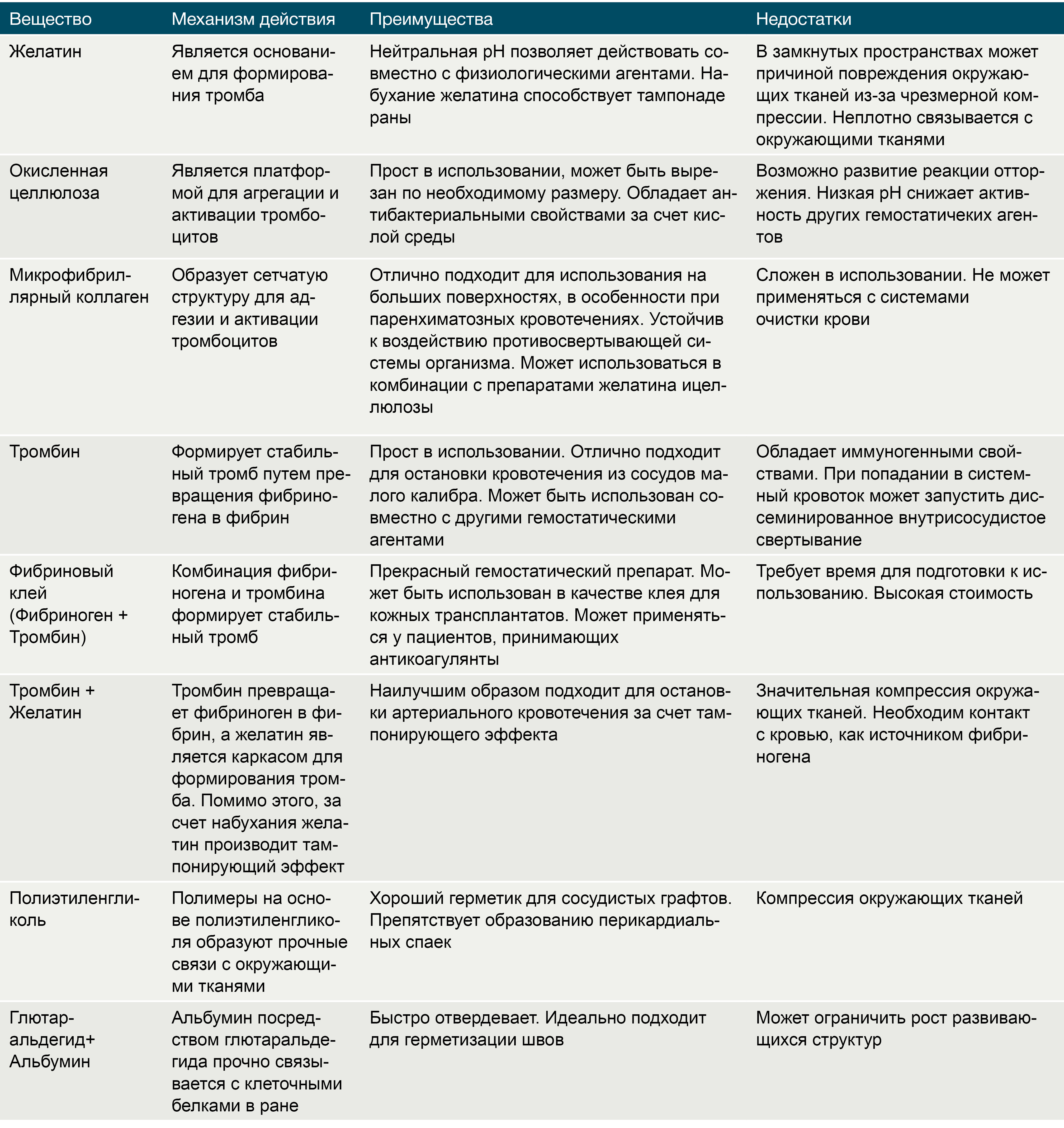 Таблица 1 | Характеристика местных гемостатиков.
Таблица 1 | Характеристика местных гемостатиков.
Источники
- Fergusson D. A. et al. A comparison of aprotinin and lysine analogues in high-risk cardiac surgery //New England Journal of Medicine. — 2008. — Т. 358. — №. 22. — С. 2319-2331.
- Williams-Johnson J. A. et al. Effects of tranexamic acid on death, vascular occlusive events, and blood transfusion in trauma patients with ificant haemorrhage (CRASH-2): a randomised, placebo-controlled trial //West Indian Medical Journal. — 2010. — Т. 59. — №. 6. — С. 612-624.
- Ferraris V. A. et al. Perioperative blood transfusion and blood conservation in cardiac surgery: the Society of Thoracic Surgeons and The Society of Cardiovascular Anesthesiologists clinical practice guideline //The Annals of thoracic surgery. — 2007. — Т. 83. — №. 5. — С. S27-S86.
- Sedrakyan A., Treasure T., Elefteriades J. A. Effect of aprotinin on clinical outcomes in coronary artery bypass graft surgery: a systematic review and -analysis of randomized clinical trials //The Journal of thoracic and cardiovascular surgery. — 2004. — Т. 128. — №. 3. — С. 442-448.
- Song H. K. et al. Safety and efficacy of prothrombin complex concentrates for the treatment of coagulopathy after cardiac surgery //The Journal of thoracic and cardiovascular surgery. — 2014. — Т. 147. — №. 3. — С. 1036-1040.
- Shapiro A. D. et al. Prospective, randomised trial of two doses of rFVIIa (NovoSeven) in haemophilia patients with inhibitors undergoing surgery //Thrombosis and haemostasis. — 1998. — Т. 79. — №. 05. — С. 773-778.
- Achneck H. E. et al. A comprehensive review of topical hemoic agents: efficacy and ations for use //Annals of surgery. — 2010. — Т. 251. — №. 2. — С. 217-228.
- McManus J. G., Wedmore I. Modern Hemoic Agents for Hemorrhage Control â A Review and ion of Use in Current Combat Operations. — 2005.
- Okuma M. et al. Effects of etamsylate on platelet s and arachidonic acid bolism //Thrombosis and haemostasis. — 1982. — Т. 48. — №. 3. — С. 330-333.
Нашли опечатку? Выделите фрагмент и нажмите Ctrl+Enter.
- Скориченко, «Доисторическая M.» (СПб., 1996); его же, «Гигиена в доисторические времена» (СПб., 1996).
- Мустафин Р. И., Буховец А. В., Протасова А. А., Шайхрамова Р. Н., Ситенков А. Ю., Семина И. И. Сравнительное исследование поликомплексных систем для гастроретентивной доставки метформина. Разработка и регистрация лекарственных средств. 2015; 1(10): 48–50.
- М.П. Киселева, З.С. Смирнова, Л.М. Борисова и др. Поиск новых противоопухолевых соединений среди производных N-гликозидов индоло[2,3-а] карбазолов // Российский онкологический журнал. 2015. № 1. С. 33-37.
- https://mosapteki.ru/material?oid=1620.
- https://medach.pro/post/1292.
- Guardia, «La Médecine à travers les âges».